Los investigadores están estudiando por qué las fábricas de energía se mueven entre las células y si el proceso se puede aprovechar para tratar el cáncer y otras enfermedades
Por: Gemma Conroy-Nature
Hay un movimiento inesperado en el mundo de la biología celular, específicamente en las fábricas de energía conocidas como mitocondrias.
Desde su descubrimiento a mediados del siglo XIX, las mitocondrias se han conocido como orgánulos que residen en el interior de las células. Pero esa imagen clásica ahora parece errónea. Un auge de investigaciones está cuestionando la imagen tradicional de las mitocondrias como orgánulos exclusivamente celulares. «Podrían ser un orgánulo multicelular», afirma Jonathan Brestoff, inmunólogo que estudia el metabolismo en la Universidad de Washington en San Luis, Misuri. En otras palabras, las supuestas fábricas de energía estáticas ahora parecen ser expertas viajeras, que se desplazan de una célula a otra según las necesidades.
Esta «transferencia mitocondrial» se ha observado en una amplia variedad de células y en organismos tan diversos como levaduras, moluscos y roedores. «Es realmente emocionante», afirma Jeffrey Spees, biólogo de células madre de la Universidad de Vermont en Burlington.
Aún no se sabe con certeza por qué las mitocondrias son tan móviles. Algunos estudios han sugerido que las células donan sus mitocondrias a sus vecinas en momentos de necesidad. En emergencias celulares, las mitocondrias recién llegadas podrían impulsar la reparación tisular, activar el sistema inmunitario o rescatar de la muerte a células en peligro. Otras investigaciones sugieren que la transferencia mitocondrial puede ser un arma letal que las células cancerosas utilizan para obtener ventaja .
Pero lo que esto significa para la salud humana sigue siendo un misterio. Los investigadores aún no han captado el proceso dentro del cuerpo humano, por lo que no saben con certeza si ocurre en las personas, afirma Daniel Davis, inmunólogo del Imperial College de Londres. «Aún no contamos con la tecnología para presenciar este fenómeno», añade.
Ese hecho no ha impedido que los investigadores exploren cómo aprovechar la transferencia mitocondrial para tratar una variedad de enfermedades, incluido el cáncer y los accidentes cerebrovasculares.
Una bacteria prestada
Durante las últimas tres décadas, las investigaciones han revelado que las mitocondrias son mucho más que centrales eléctricas celulares que transforman los nutrientes de los alimentos en energía. Son actores clave en múltiples procesos del cuerpo: guían el funcionamiento celular y contribuyen a la respuesta inmunitaria contra invasores dañinos. Además, presentan una diversidad sorprendente. El año pasado, investigadores descubrieron que las mitocondrias se dividen en dos formas distintas para ayudar a las células a sobrevivir a la carencia de nutrientes 1 . Otro estudio, publicado en marzo, modeló la densidad y el tipo de mitocondrias en todo el cerebro humano 2.
Se cree que todas las mitocondrias, en cualquier organismo y en cualquier parte del cuerpo, provienen de la misma bacteria ancestral. Hace unos 1500 millones de años, esta bacteria errante fue absorbida por el microbio que finalmente dio origen a los eucariotas, el gran grupo de organismos, incluyéndonos a nosotros, cuyas células tienen un núcleo cerrado.
Tras varios altibajos evolutivos, esta bacteria prestada se convirtió en el orgánulo que impulsa el metabolismo . El origen microbiano de las mitocondrias probablemente explica por qué son más dinámicas de lo que parecen a primera vista, afirma Kazuhide Hayakawa, neurocientífico del Hospital General de Massachusetts en Boston, quien estudia cómo la transferencia mitocondrial podría ayudar en el tratamiento del ictus. «Es posible que las mitocondrias conserven la antigua capacidad de propagarse de una célula a otra, como las bacterias», afirma.
En 2006, Spees y sus colegas captaron por primera vez el paso de las mitocondrias entre células. El equipo había estado intentando comprender el desconcertante comportamiento de las células madre en placas de laboratorio. Estas células parecían compartir información física que les indicaba cómo diferenciarse, y se creía que las mitocondrias estaban implicadas.
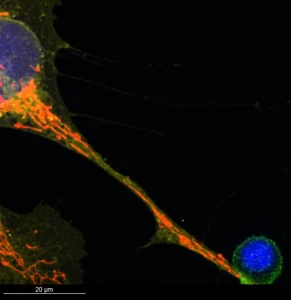
Para investigar la función de las mitocondrias, los investigadores cultivaron células de cáncer de pulmón humano, que carecían de orgánulos, con células madre de médula ósea. Con las mitocondrias de las células madre marcadas con proteínas fluorescentes, el equipo grabó un video a cámara rápida de lo que sucedió a continuación.
Las imágenes granuladas en blanco y negro mostraban cómo las células madre liberaban sus mitocondrias, que luego eran absorbidas por las células pulmonares defectuosas. Tras la donación, las células pulmonares recuperaron rápidamente su capacidad de dividirse y transformar la glucosa en energía. «Observarlo fue como un milagro», afirma Spees.
Desde entonces, los investigadores han observado el desplazamiento rápido de las mitocondrias entre varios tipos de células: pulmón, corazón, cerebro, tejido adiposo, hueso y más. En ocasiones, las mitocondrias recorren vías efímeras conocidas como nanotubos túnel que se forman entre las células y transportan otra carga celular. En otros casos, las mitocondrias realizan su viaje en vesículas con forma de burbuja o flotan libremente en la sangre 4 (véase «Tres maneras de viajar»).
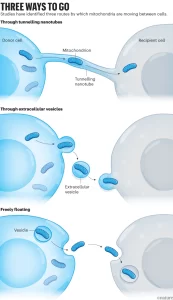
El mecanismo de desplazamiento de las mitocondrias está prácticamente resuelto, pero lo que no está tan claro es el motivo. Los investigadores están descubriendo que este proceso suele ser una forma de control del daño celular, afirma Clair Crewe, bióloga celular de la Universidad de Washington.
Algunos estudios sugieren, por ejemplo, que la transferencia mitocondrial podría ayudar a las células a capear tormentas neurológicas. En 2016, Hayakawa y sus colegas descubrieron que en ratones que habían sufrido un derrame cerebral, las células de soporte llamadas astrocitos entregan sus mitocondrias a las neuronas vacilantes. Con este impulso mitocondrial, las neuronas desarrollaron ramas y reiniciaron sus procesos metabólicos, lo que mejoró sus posibilidades de supervivencia. Cuando los investigadores inhibieron la transferencia mitocondrial, sobrevivieron menos neuronas, lo que sugiere que los orgánulos donados fueron clave para la recuperación de las células 5 . Pero qué parte de la estructura o función de las mitocondrias protegió a las células sigue siendo desconocida, dice Hayakawa.
Las células pulmonares también podrían beneficiarse de un refuerzo mitocondrial durante una crisis, afirma Jahar Bhattacharya, de la Universidad de Columbia en la ciudad de Nueva York, especializado en una afección inflamatoria grave conocida como lesión pulmonar aguda. Él y sus colegas han descubierto que, en ratones con esta inflamación, las células del estroma (que componen los tejidos conectivos que sostienen los órganos) transfieren sus mitocondrias a las células pulmonares . Las células con orgánulos prestados presentaron mayores concentraciones de ATP, el combustible celular, que finalmente se distribuyó a las células cercanas que no recibieron nuevas mitocondrias.
Estos pulmones enfermos mostraron más signos de recuperación que los pulmones enfermos que no recibieron mitocondrias externas. Bhattacharya se sorprendió cuando él y su equipo presenciaron la transferencia mitocondrial en acción. «No creo que hayamos dormido en las siguientes noches; fue muy emocionante», dice.
Otras investigaciones sugieren que la transferencia de mitocondrias podría acelerar la cicatrización de heridas. En 2021, Anne-Marie Rodriguez, bióloga celular de la Universidad de la Sorbona en París, y sus colegas descubrieron que las plaquetas aisladas de sangre humana transportaron sus mitocondrias a células madre cuando los investigadores combinaron ambos tipos de células en una placa de cultivo. Tras absorber las mitocondrias, las células madre liberaron moléculas que participan en la formación de nuevos vasos sanguíneos. Cuando las células se colocaron sobre heridas cutáneas en ratones, estas heridas cicatrizaron más rápido que en roedores que habían recibido solo células madre o plaquetas .
Los investigadores sospechan que las células con mitocondrias disfuncionales podrían incluso tener formas de solicitar mitocondrias sanas a sus vecinas, aunque los mecanismos exactos que subyacen a este proceso siguen siendo inciertos. «Apenas estamos empezando a comprender la señalización implicada», afirma Crewe.
Operaciones cotidianas
Más allá de su papel en la recuperación, los investigadores quieren saber si la transferencia mitocondrial es una parte esencial de la biología cotidiana. La evidencia inicial sugiere que podría ayudar a mantener los tejidos sanos. El año pasado, Minghao Zheng, un biólogo regenerativo de la Universidad de Australia Occidental en Perth, y sus colegas descubrieron que algunos tipos de astrocitos donan sus mitocondrias a las células que recubren los vasos sanguíneos en el cerebro del ratón 8 . Cuando los investigadores interrumpieron este proceso, la barrera hematoencefálica se volvió permeable, lo que sugiere que la transferencia mitocondrial ayuda a mantener este escudo de membrana protectora. Zheng y su equipo ya habían informado que la transferencia mitocondrial en los huesos de los ratones puede acelerar la formación de nuevos vasos sanguíneos 9 .
En ratones sanos, Brestoff y sus colegas informaron que los glóbulos blancos transfieren sus mitocondrias a los macrófagos, glóbulos blancos que absorben los restos celulares. El número de orgánulos transportados se redujo en los ratones obesos. Los ratones obesos también consumieron menos energía que sus contrapartes sanas . 10 Estos orgánulos podrían ayudar a los macrófagos a funcionar cuando su metabolismo se ve alterado, afirma Brestoff.
En el complejo mundo del sistema inmunitario, las mitocondrias donadas podrían tener un efecto antiinflamatorio, especialmente cuando son absorbidas por los linfocitos T (glóbulos blancos que previenen infecciones y enfermedades). En estudios con cultivos celulares, Patricia Alejandra Luz-Crawford, inmunóloga de la Universidad de los Andes en Santiago de Chile, y sus colegas descubrieron que algunos tipos de linfocitos T que reciben mitocondrias de células madre producen menos moléculas inflamatorias. Las células madre cultivadas de personas con artritis reumatoide transfieren menos mitocondrias a los linfocitos T que las células madre de individuos sanos, lo que, según ella, podría contribuir a la inflamación crónica asociada con la enfermedad.
Pero aún quedan muchas preguntas sin respuesta sobre la transferencia mitocondrial, incluyendo qué podrían estar haciendo los orgánulos tras entrar en las células y cuánto duran, afirma Luz-Crawford. «Aún hay mucho misterio».




