Equipadas con anticuerpos que las guían al sitio del tumor, las nuevas nanopartículas podrían reducir los efectos secundarios del tratamiento
Anne Trafton | Noticias del MIT
Utilizando partículas diminutas con forma de cepillos para botellas, los químicos del MIT han descubierto una forma de administrar una amplia gama de medicamentos de quimioterapia directamente a las células tumorales.
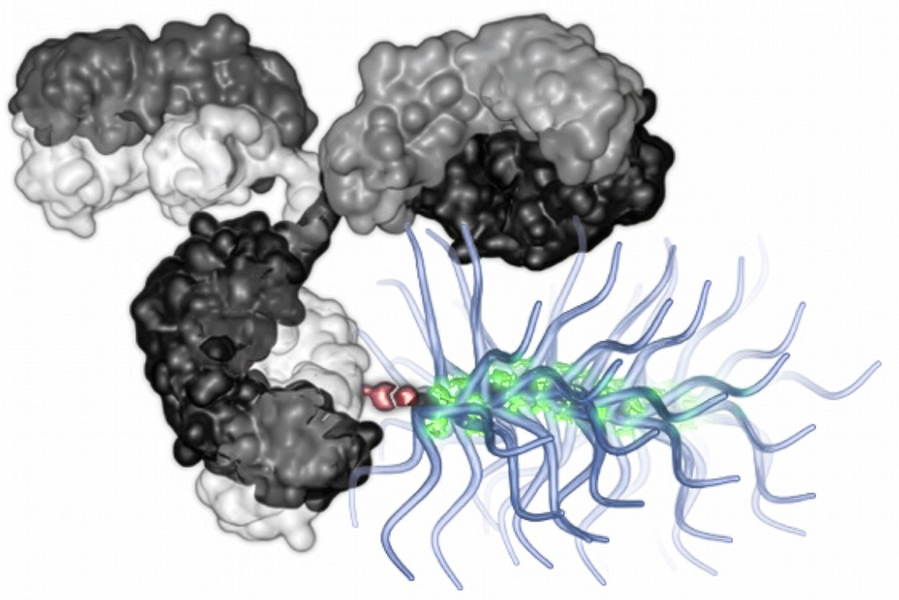
Para guiarlas a la ubicación correcta, cada partícula contiene un anticuerpo dirigido contra una proteína tumoral específica. Este anticuerpo está unido a cadenas de polímero con forma de cepillo de botella que transportan docenas o cientos de moléculas de fármaco, una carga mucho mayor que la que puede administrar cualquier conjugado anticuerpo-fármaco existente.
En modelos murinos de cáncer de mama y ovario, los investigadores descubrieron que el tratamiento con estas partículas conjugadas podía eliminar la mayoría de los tumores. En el futuro, las partículas podrían modificarse para atacar otros tipos de cáncer mediante la incorporación de diferentes anticuerpos.
“Estamos entusiasmados con el potencial de abrir un nuevo panorama de cargas útiles y combinaciones de cargas útiles con esta tecnología, que en última instancia podría proporcionar terapias más efectivas para pacientes con cáncer”, dice Jeremiah Johnson, profesor de Química A. Thomas Geurtin en el MIT, miembro del Instituto Koch para la Investigación Integral del Cáncer y autor principal del nuevo estudio.
Una mayor carga de droga
Los conjugados anticuerpo-fármaco (ADC) son un tipo prometedor de tratamiento contra el cáncer que consiste en un anticuerpo dirigido contra el cáncer unido a un fármaco quimioterapéutico. La FDA ha aprobado al menos 15 ADC para tratar diversos tipos de cáncer.
Este enfoque permite la focalización específica de un fármaco contra el cáncer en un tumor, lo que ayuda a prevenir algunos de los efectos secundarios que se producen cuando los fármacos de quimioterapia se administran por vía intravenosa. Sin embargo, una desventaja de los ADC actualmente aprobados es que solo unas pocas moléculas de fármaco pueden unirse a cada anticuerpo. Esto significa que solo pueden usarse con fármacos muy potentes, generalmente agentes que dañan el ADN o fármacos que interfieren con la división celular.
Para intentar utilizar una gama más amplia de fármacos, que suelen ser menos potentes, Johnson y sus colegas decidieron adaptar las partículas de cepillo de botella que habían inventado previamente. Estas partículas consisten en una estructura polimérica unida a decenas o cientos de moléculas de «profármaco»: moléculas farmacológicas inactivas que se activan al liberarse en el organismo. Esta estructura permite que las partículas administren una amplia gama de moléculas farmacológicas, y pueden diseñarse para transportar múltiples fármacos en proporciones específicas.
Mediante una técnica llamada química de clic, los investigadores demostraron que podían unir uno, dos o tres de sus polímeros de cepillo de botella a un solo anticuerpo dirigido contra un tumor, creando un conjugado anticuerpo-cepillo de botella (ABC). Esto significa que un solo anticuerpo puede transportar cientos de moléculas de profármaco. Los ADC actualmente aprobados pueden transportar un máximo de aproximadamente ocho moléculas de fármaco.
La enorme cantidad de cargas útiles en las partículas ABC permite a los investigadores incorporar medicamentos contra el cáncer menos potentes, como la doxorrubicina o el paclitaxel, lo que mejora la capacidad de personalización de las partículas y la variedad de combinaciones de medicamentos que se pueden utilizar.
“Podemos usar conjugados de anticuerpo-cepillo de botella para aumentar la carga farmacológica y, en ese caso, podemos usar fármacos menos potentes”, afirma Liu. “En el futuro, podremos copolimerizar fácilmente con múltiples fármacos para lograr una terapia combinada”.
Las moléculas del profármaco se unen a la estructura principal del polímero mediante enlaces escindibles. Tras alcanzar el tumor, algunos de estos enlaces se rompen inmediatamente, lo que permite que los fármacos destruyan las células cancerosas cercanas, incluso si no expresan el anticuerpo diana. Otras partículas son absorbidas por las células con el anticuerpo diana antes de liberar su carga tóxica.
Tratamiento eficaz
Para este estudio, los investigadores crearon partículas ABC que transportaban diferentes tipos de fármacos: inhibidores de microtúbulos llamados MMAE y paclitaxel, y dos agentes que dañan el ADN, doxorrubicina y SN-38. También diseñaron partículas ABC que transportaban un tipo experimental de fármaco conocido como PROTAC (quimera dirigida a la proteólisis), que puede degradar selectivamente las proteínas patógenas dentro de las células.
Cada cepillo para botella estaba conectado a un anticuerpo dirigido a HER2, una proteína que a menudo se sobreexpresa en el cáncer de mama, o a MUC1, que se encuentra comúnmente en el cáncer de ovario, de pulmón y otros tipos de cáncer.
Los investigadores probaron cada una de las partículas ABC en modelos murinos de cáncer de mama o de ovario y descubrieron que, en la mayoría de los casos, las partículas ABC lograron erradicar los tumores. Este tratamiento fue significativamente más eficaz que administrar los mismos profármacos de tipo cepillo de botella por inyección, sin estar conjugados con un anticuerpo diana.
“Utilizamos una dosis muy baja, casi 100 veces menor en comparación con el fármaco tradicional de molécula pequeña, y el ABC aún puede lograr una eficacia mucho mejor en comparación con el fármaco de molécula pequeña administrado por sí solo”, afirma Liu.
Estos ABC también tuvieron un mejor rendimiento que dos ADC aprobados por la FDA, T-DXd y TDM-1, que utilizan HER2 para dirigirse a las células. T-DXd contiene deruxtecán, que interfiere con la replicación del ADN, y TDM-1 contiene emtansina, un inhibidor de microtúbulos.
En trabajos futuros, el equipo del MIT planea probar combinaciones de fármacos que actúen mediante diferentes mecanismos, lo que podría mejorar su eficacia general. Entre estos podrían incluirse fármacos de inmunoterapia como los activadores de STING.
Los investigadores también están trabajando en la incorporación de diferentes anticuerpos, como los dirigidos contra el EGFR, ampliamente expresado en numerosos tumores. Se han aprobado más de 100 anticuerpos para tratar el cáncer y otras enfermedades, y en teoría, cualquiera de ellos podría conjugarse con fármacos contra el cáncer para crear una terapia dirigida.